
为什么有的蛋白电泳呈现清晰单一条带,有的却能观察到完整复合物?为什么有的实验需要加热煮沸,有的却必须低温操作?答案在于凝胶系统的选择——非变性电泳(Native-PAGE) 与 变性电泳(SDS-PAGE)。两者基于相同原理,却在分离机制和应用场景上有着本质区别。
本文将分上下两篇,系统解析两种技术的异同,并整理非变性电泳实操全攻略,助您一步到位掌握核心要点。
两种技术的核心差异
蛋白质在电泳过程中保持其天然构象,迁移速率由天然电荷密度、分子大小和空间构象共同决定。其中,蛋白质的等电点(pI) 是最关键的调控因素。由于体系中不含SDS等变性剂,蛋白质的固有电荷未被掩盖,因此不同蛋白质的电荷异质性得以保留,迁移行为由其综合物化属性决定。
1.2 SDS-PAGE
在阴离子去垢剂SDS存在下,蛋白质被完全变性并解聚为多肽链。SDS以恒定比例(1.4 g SDS / g 蛋白)与蛋白质结合,有效屏蔽蛋白质的固有电荷,使所有蛋白质-SDS复合物均带有均匀的负电荷密度。同时,SDS诱导蛋白质从天然构象转变为无规卷曲/长杆状,消除了形状对迁移的影响。最终,蛋白质的迁移速率仅与其分子量的对数呈线性相关——分子量越小,迁移距离越大。
2.1 Native-PAGE
• 蛋白质状态:保持天然三维构象,生物活性得以保留,亚基间相互作用及寡聚化状态完整。
• 电荷特征:蛋白质携带其固有净电荷。大多数蛋白质的等电点(pI)在3-8之间,在常规Tris-甘氨酸缓冲体系(pH ~8.3)中带负电,因此向阳极迁移;若蛋白质pI>7(碱性蛋白),则需反转电极极性以实现有效分离。
• 可观测信息:可直接解析蛋白质的天然寡聚状态(如单体、二聚体、多聚体)及蛋白质复合物组成,电泳后还可进行原位酶活性染色或同工酶分析。
2.2 SDS-PAGE
• 蛋白质状态:完全变性、解聚为多肽链,天然构象及生物活性丧失。
• 电荷特征:所有蛋白质-SDS复合物均带负电荷,因此在电场中均向阳极迁移。
• 可观测信息:获得单一亚基的清晰条带,可根据条带相对迁移距离推算表观分子量,适用于蛋白质表达分析、纯度鉴定等。
3.1 Native-PAGE
• 天然蛋白质复合物的分离与分析:从组织匀浆或膜组分中一步分离具有生物学活性的蛋白质复合物。
• 寡聚状态及相互作用研究:确定蛋白质的天然分子量、亚基组成及生理条件下的蛋白质-蛋白质相互作用。
• 功能活性检测:电泳后直接进行酶活性染色、配体结合分析等功能性实验。
• 结构生物学样品制备:从凝胶中回收天然蛋白质复合物,用于二维结晶、负染电镜等结构解析前处理。
3.2 SDS-PAGE
• 分子量测定:根据标准曲线计算蛋白质亚基的表观分子量。
• 蛋白质表达分析:检测目标蛋白质的表达水平、诱导表达效果及样品间差异。
• Western blot前处理:变性后的蛋白质更易于与抗体结合,是免疫印迹实验的标准流程。
• 纯度评估:监测蛋白质纯化过程中各流份的纯度和降解情况。
4.1 Native-PAGE
✅ 保留蛋白质天然构象与活性,可获得功能相关的结构信息
✅ 支持电泳后直接进行功能检测,无需额外复性步骤
❌ 实验条件需优化(如缓冲液pH、凝胶浓度、电极方向),操作复杂度较高
❌ 迁移行为受多重因素影响,无法直接推算分子量
4.2 SDS-PAGE
✅ 操作标准化程度高,实验重复性好,适用范围广
✅ 分子量测定准确,数据易于定量分析
✅ 样品处理简单(热变性即可),适合高通量分析
❌ 蛋白质完全变性,无法获得天然构象及功能相关信息

非变性电泳(Native-PAGE)操作全攻略
关键要点:
• 所有的预染蛋白Marker均为SDS-PAGE设计,不适用于非变性电泳。
• 非变性条件下,蛋白质迁移受电荷、形状和分子量共同影响,因此在单一凝胶浓度下,非变性蛋白Marker无法精确推算目标蛋白的分子量。
• 如需确定非变性条件下蛋白质的分子量,应在不同凝胶浓度下测定蛋白质的相对迁移率(Rf值),绘制凝胶浓度对Rf的曲线进行推算。
• 非变性蛋白专用Marker为保持天然结构,均未偶联染料,电泳过程中不可见。如需检测非变性蛋白Marker的转膜效果,可使用丽春红染色液,但需注意其灵敏度较低,可能无法显示完整条带。
推荐产品: MKPZ010 非变性蛋白 Marker (66-669 kDa)
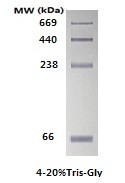
关键要点:
• 必须使用非变性上样缓冲液,确保不含SDS、DTT等变性剂。
• 严禁加热样品,室温或冰上操作即可,避免热诱导变性。
关键要点:
• 凝胶和电泳缓冲液中均不得添加SDS。
• 常规蛋白质(pI 3-8)按常规方向电泳(向阳极迁移);若目标蛋白pI>7(碱性蛋白),需反转电极电泳,常规蛋白(pI<7)按常规向阳极迁移;
• 电泳过程中产热可能导致蛋白质变性,建议在电泳槽外置冰浴降温。
• 非变性条件下蛋白质分子量较大,推荐使用5%-10%的凝胶浓度。
• 非变性蛋白质荷质比较低,泳动速度较慢,需适当延长电泳时间。
关键要点:
• 转膜缓冲液中的甲醇对蛋白质有固定作用,非变性转膜应少加或不加甲醇。
• 以下转膜条件为通用参考值,建议根据目标蛋白特性进行1-2次预实验优化:
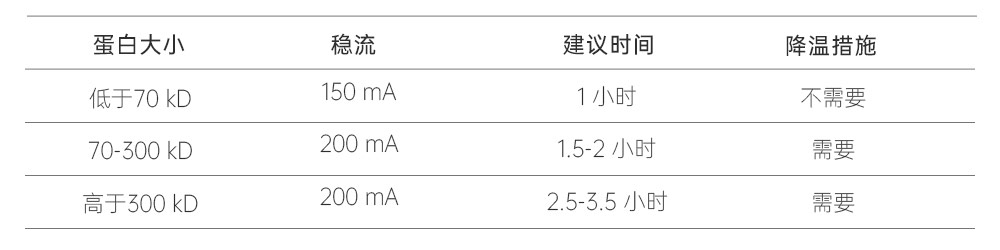
• 膜孔径选择:>20 kD蛋白选用0.45 μm孔径,≤20 kD蛋白选用0.22 μm孔径。PVDF膜使用前需用无水甲醇润湿活化。

只要抓住 “保留天然状态” 这一核心,严格把控样品、电泳、转膜的每一个细节,避开变性雷区,非变性电泳也能轻松做好。
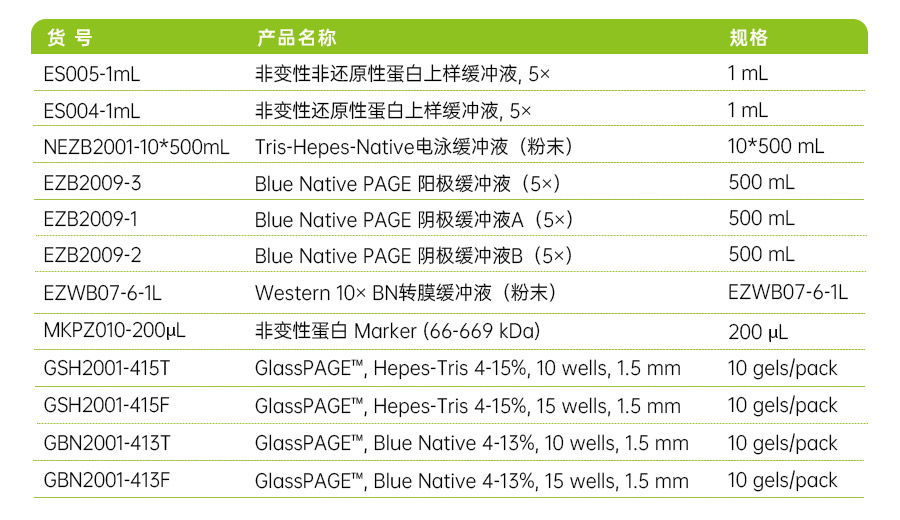
万生昊天 GlassPAGE™ 和 PlusPAGE™ 预制胶系列产品本身不含SDS,通过选择不同电泳缓冲液即可实现变性/非变性模式的自由切换,为您的实验设计提供更大灵活性。
Native-PAGE 与 SDS-PAGE:前者解析天然状态,后者聚焦分子量信息。
明确实验目的,选择适配方法,方能获得可靠的实验结果。
万生昊天生物,专注高品质预制胶与电泳解决方案,助您科研之路事半功倍。

读完这篇干货,你对Native-PAGE和SDS-PAGE的区别是否更清晰了?欢迎在评论区留言交流:
📌你在实验中选择Native-PAGE还是SDS-PAGE?主要研究什么类型的蛋白?
📌做非变性电泳时,你遇到过哪些“翻车”经历?如何解决的?
📌关于蛋白电泳,你还有哪些想了解的专题?
🎁 精选留言奖励:我们将抽取3位读者,送出万生昊天实验周边(签字笔/笔记本)!

1. ➡️关注“万生昊天生物”公众号,领取实验资料包 。
2. 加入实验交流群
👥扫码添加小助手微信(ID: wshtbio-Inc),备注“WB+单位”,即可进入蛋白实验技术交流群,与同行实时讨论!
3. 往期精选推荐
📚 如果你觉得本文有用,可能也会喜欢:
